铬(Ⅵ)的方波伏安行为和测定
| 论文类型 | 基础研究 | 发表日期 | 2004-06-01 |
| 来源 | 《工业用水与废水》2004年第3期 | ||
| 作者 | 许琦,严金龙,杨春生 | ||
| 关键词 | 方波伏安法 铬(Ⅵ) 废水测定 环境分析 | ||
| 摘要 | 在0.1 mol/L的氨水缓冲溶液(pH=10.0)中,铬(Ⅵ)离子于-1.45V(vs S.C.E)出现一灵敏的方波伏安峰。峰电流Ip与Cr(Ⅵ)的质量浓度在0.1~2.0× 103m/L范围内呈现良好的线性关系,其相关系数为0.9886,检出限为0.05mg/L Cr(Ⅵ),方法的标准偏差为2.8%。该法应用于实际样品电镀铬液及其废液中铬(Ⅵ)含量的测定,结果表明:与标准方法二苯碳酰二肼分光光度法比较,本法不需要加入特定的试剂而直接水样测定,简单快速。 | ||
许琦,严金龙,杨春生
(盐城工学院 化学工程系,江苏 盐城 224003)
摘要:在0.1 mol/L的氨水缓冲溶液(pH=10.0)中,铬(Ⅵ)离子于-1.45V(vs S.C.E)出现一灵敏的方波伏安峰。峰电流Ip与Cr(Ⅵ)的质量浓度在0.1~2.0× 103m/L范围内呈现良好的线性关系,其相关系数为0.9886,检出限为0.05mg/L Cr(Ⅵ),方法的标准偏差为2.8%。该法应用于实际样品电镀铬液及其废液中铬(Ⅵ)含量的测定,结果表明:与标准方法二苯碳酰二肼分光光度法比较,本法不需要加入特定的试剂而直接水样测定,简单快速。
关键词:方波伏安法;铬(Ⅵ);废水测定;环境分析
中图分类号:X830.2 文献标识码:B 文章编号:1009-2455(2004)03-0051-03
Square-Wave Voltampere Behavior of Cr(Ⅵ) Ion and Its Determination
Xu Qi,YAN Jin-long,YANG Chun-sheng
(Department of Chemical Engineering,Yancheng Institute of Technology,Yancheng 224003,China)
Abstract:Chromium (Ⅵ) ion showed a sensitive square-wave voltampere peak at -1.45 V(vs S.C.E) in the buffer solution of 0.1 mol/L ammonia liquor (pH=10.0).There appeared a good linear relationship between the peak current Ip and the mass concentration of Cr(Ⅵ) when it was within the range of 0.1~2.0×103mg/L,the correlation coefficient of which was 0.9886,the detection limit was 0.05 mg/L Cr(Ⅵ),and the standard deviation was 2.8%.The said method was used in determining the chrome (Ⅵ) contents in the sample of actual chrome plating solution and the waste liquor,the results of which showed that compared with spectrophotography with 1,5-Diphenylcarbohydrazide,which is a standard method,this method does not need the addition of specific reagent but directly determines the water sample,which is simple and quick.
Key words:square-wave voltampere method;chromium (Ⅵ);wastewater determination;environmental analysis
环境中的铬主要以无机铬和有机铬两种形态存在,其中无机铬的含量远比有机铬大得多,而无机铬中常见的形态为铬(Ⅲ)和铬(Ⅵ)。铬及其化合物在工业中应用广泛,能够以各种形式进入环境。有关工厂的废水、废气排放都对环境造成了较大的污染,是环境污染监测中的必测项目之一。因此,研究一种简单、快速而准确测定铬(Ⅵ)离子的方法就显得非常的重要[1-3]。
到目前为止,已报道了许多测定环境中铬(Ⅵ)的方法。主要有分光光度法、原子光谱分析法等[4-6],但有的试剂选择性较差,用于某些复杂样品分析时,常需借助适当的分离富集手段以消除干扰,有的仪器设备复杂。电化学分析法虽然有报道,但体系复杂,一般是采用极谱催化波或络合吸附波,分析时通过选择合适的氧化还原体系改变铬的存在价态,结合特定的研究方法测定总量,采用差减法测定各单一价态铬的含量[4]。而分光光度法是国内外的标准方法,利用在酸性介质中,六价铬与二苯碳酰二肼(DPC)反应,生成紫红色络合物,于540nm波长处进行比色测定[1]。
本文研究了铬(Ⅵ)在NH3-NH4C1(pH=10.0)介质条件下的电化学行为,并依此建立了方波伏安法快速分析环境中的铬(Ⅵ),方法的线性范围为0.1~2.0×103mg/L,检出限为0.05mg/L,方法简单、快速,应用于实际样品电镀铬液及其废液中铬(Ⅵ)含量的测定,结果满意。
1 实验部分
1.1 主要仪器及试剂
CHI832电化学分析仪;三电极系统:汞膜电极为工作电极,铂电极为辅助电极,甘汞电极为参比电极;SRD-1型磁力搅拌器。
铬标准溶液:5.0g/L,准确称取基准重铬酸钾1.25g于100mL烧杯中,少量蒸馏水溶解,转移到250mL容量瓶中,并定容。其它浓度的溶液,由此溶液稀释所得。
氨水缓冲溶液(pH=10.0):1 mol/L,将54gNH4Cl溶于水中,加人浓氨水350mL,稀释 1.OL。
饱和Na2SO3溶液。
试剂皆为分析纯,水为二次蒸馏水。
1.2 试验方法
准确移取氨水缓冲溶液2.00mL于20mL比色管中,加入饱和Na2SO3溶液4.00mL和一定量的铬标准溶液,定容后搅拌除氧10min。插入电极,控制起始电位为 -1.00 V,负向扫描 -1.6V,在电化学分析仪上记录方波伏安峰,测其在 -1.45V(vs S.C.E,相对于饱和甘汞电极,下同)处的方波伏安电流峰高Ip。
2 结果与讨论
2.1 铬的方波伏安峰
在O.1 mol/L的氨水缓冲溶液中,Cr(Ⅵ)在汞膜电极上于 -1.45V(vs S.C.E)处出现一灵敏的方波伏安峰,伏安图波形较好,且峰电流Ip与Cr(Ⅵ)的浓度在一定的范围内呈线性关系,而氨水缓冲溶液底液无峰(见图1)。
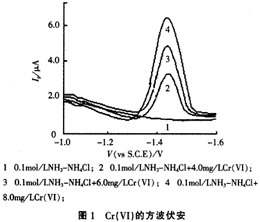
方波伏安技术用于物质的测定,具有灵敏度高、分辨率好、前波影响小等特点,图1结果表明:将其用于Cr(Ⅵ)的定量分析,缓冲底液、溶解氧及其它杂质对Cr(Ⅵ)方波伏安峰均无干扰,峰型对称,利于测定。
2.2 支持电解质的选择
考察了Cr(Ⅵ)在不同浓度和pH值的NH3-NH4Cl缓冲溶液、硼砂缓冲溶液、KOH溶液、KCl、B-R缓冲溶液等多种缓冲体系中的伏安行为,发现仅在氨水缓冲体系中波形良好、灵敏度高。氨水溶液浓度≥5.0× 10-3mol/L时,伏安峰灵敏且稳定,本法选择0.1 mol/L,氨水溶液作为测定介质。
2.3 电化学实验条件的选择
随着方波频率增大,金属离子峰电流逐渐增大,峰电位负移,但半峰宽也增大,对测定不利,本法选择频率为35Hz。静止时间在10s之后,波峰达到最大且稳定,本法选取静止时间为10s,电位扫描速度为4mV/s。
起始电位在 -0.8~-1.1V之间时,峰电流基本不变化,本实验选择-1.0V作为测定的起始电位。
2.4 循环伏安图
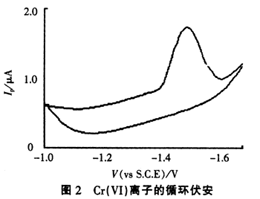
在0.1 mol/L的氨水缓冲溶液中,质量浓度为5.0mg/LCr(Ⅵ)离子的循环伏安图示于图2。循环伏安图表明在阴极分支上有还原峰,阳极分支无氧化峰,说明Cr(Ⅵ)离子在汞膜电极上的电极反应过程为不可逆过程。
2.5 线性范围和检出限
在上述最佳条件下,峰电流Ip与Cr(VI)的质量浓度在0.1~2.0×103mg/L范围内呈现良好的线性关系,其回归方程为Ip(μA)=0.2870+0.6424C(mg/L),相关系数为0.9886,检出限为ρ(Cr6+)=0.05mg/L。
2.6 共存离子的影响
pH=10.0的氨水缓冲溶液中,ρ(Cr6+)=5.0mg/L条件下,相对误差≤±5%时,允许以下离子(倍数)共存:K+,Na+,Al3+,NH4+,Mg2+,Ca2+,NO3-, SO42-(5.0× 103), Mn2+(1000), Cu2+(500),Fe3+(350), Cr3+(210), Cd2+(175), Fe2+(142), Zn2+(50)不影响测定。
2.7 合成水样分析
对质量浓度为5.0mg/L Cr(Ⅵ)的合成标准样进行了6次平行测定,方法的相对标准偏差为2.8%,说明实验所建立的方法具有很高的精密度,结果见表1。
表1 合成水样分析结果
合成样品
ρ(Cr6+)/(mg·L-1)
测定值
ρ(Cr6+)/(mg·L-1)
平均测定值
ρ(Cr6+)/(mg·L-1)
相对标准偏差/%
5.0
4.92
4.98
4.98
5.02
2.8 5.04 5.10 5.10
2.8 电镀废液和镀铬溶液中Cr(Ⅵ)分析
吸取适量样品溶液并调节pH值近中性,经阳离子交换树脂处理后,溶液于25 mL容量瓶中定容。准确移取适量溶液于电解池中,按实验方法进行测定。并于二苯碳酰二肼标准方法测定结果进行对照,表明无显著性差异,结果见表2。
表2 样品分析结果
样品
ρ(Cr6+)/(mg·L-1)
回收率/%
本法
标准法
加入量
本法总量
电镀废液1
1.08
1.12
1.00
2.07
99.0
电镀废液2
2.84
2.90
2.00
4.85
100.5
渡铬溶液
198.6
200.4
100.0
300.2
101.6
*表中所有的分析结果皆为6次分析结果的平均值。
参考文献:
[1] 蔡宏道.环境污染与卫生监测[M].北京:人民卫生出版社,1981.
[2] 康新平,刘洪海,陈坚.液体样品中铬的价态和微量分析的研究进展[J].理化检验-化学分册,1999,35(3):139-142.
[3] 柴之芳,祝汉民.微量元素化学概论[M].北京:原子能出版社,1994.
[4] 魏显有,王秀敏,刘云惠,等.铬(Ⅵ)-硫脲体系的极谱吸附波及其应用于土壤中总铬和有效铬(Ⅵ)的测定[J].分析化学,1996, 24(10): 1170-1174.
[5] 冯素玲,唐安娜,樊静.荧光分析法测定痕量铬Ⅵ[J].分析化学,2001,29(5):558-560.
[6] 严金龙.用甲壳素富集光度法测定废水中的微量铬离子[J].材料保护,2001,34(11):39-40.
作者简介:许琦(1965-),男,江苏盐城人,副教授,博士,现 主要从事化工机械及环保有关的教学、科研工作。
论文搜索
月热点论文
论文投稿
很多时候您的文章总是无缘变成铅字。研究做到关键时,试验有了起色时,是不是想和同行探讨一下,工作中有了心得,您是不是很想与人分享,那么不要只是默默工作了,写下来吧!投稿时,请以附件形式发至 paper@h2o-china.com ,请注明论文投稿。一旦采用,我们会为您增加100枚金币。








